Soal UTBK 2019 Kimia + Pembahasan
Soal UTBK 2019 Kimia dan Pembahasan - Berikut soal dan pembahasan UTBK Kimia tahun 2019.
Diketahui profil reaksi kesetimbangan antara A, B, dan C pada suhu tertentu sebagai berikut.
Reaksi kesetimbangan yang sesuai untuk grafik di atas adalah ...
(A) 4A ⇌ 4B + 3C
(B) A + C ⇌ 2B
(C) A ⇌ 2B + C
(D) A ⇌ 4B + 2C
(E) 5A ⇌ 2B + 4C
Molekul ClF3 memiliki 3 domain pasangan elektron ikatan dan 2 domain pasangan elektron bebas. Bentuk molekul dari ClF3 adalah...
(A) tetrahedron terdistorsi.
(B) bipiramida trigonal.
(C) bentuk T.
(D) linier.
(E) piramida segi empat.
Untuk menjawab soal No. 3 sampai dengan Soal No. 5 gunakan keterangan berikut:
Sebanyak 50 mL larutan SO2 dititrasi dengan larutan
KBrO4 0,1 M menurut reaksi:
KBrO4 + 4SO2 + 4H2O → 4H2SO4 + KBr
Titik ekivalen tercapai saat volume KBrO4 yang digunakan sebanyak 50 mL.
Konsentrasi SO2 dalam larutan adalah ...
(A) 0,1 M
(B) 0,2 M
(C) 0,3 M
(D) 0,4 M
(E) 0,5 M
Jumlah mol elektron yang terlibat dalam reaksi di atas adalah...
(A) 0,02 mol
(B) 0,04 mol
(C) 0,08 mol
(D) 0,10 mol
(E) 0,12 mol
pH larutan setelah titrasi adalah ...
(A) 4
(B) 4 - log 2
(C) 4 - 2log 2
(D) 1 - log 2
(E) 1 - 2log 2
Pernyataan yang benar tentang grafik di atas adalah...
(A) A + B bisa langsung membentuk P.
(B) A + B membentuk P melalui dua kompleks teraktifkan yaitu AB* dan C*.
(C) Reaksi A + B → P melepaskan energi sebesar (E – F).
(D) Reaksi A + B → P melepaskan energi sebesar (F – D).
(E) Reaksi A + B → C adalah reaksi eksoterm.
Sebanyak 20 mL larutan $KMnO_4$ 0,2 M tepat bereaksi dengan 80 mL larutan $H_2C_2O_4$ sesuai persamaan kimia :
$2MnO_4^{-}$ + $5C_2O_4^{2-}$ + $16H^+ \rightarrow Mn^{2+}$ + $10CO_2$ + $8H_2O$. Volume gas $CO_2$ yang dihasilkan diukur pada 0°C dan 76 cmHG adalah ...
(A) 0,112 L
(B) 0,224 L
(C) 0,336 L
(D) 0,448 L
(E) 0,560 L
per butir = 0,1 mmol
$pK_a = 4$
Kondisi awal
Berdasarkan ilustrasi molekular di atas, apabila spesi-spesi tersebut dibiarkan bereaksi, ilustrasi molekular yang membentuk larutan penyangga adalah ...
(A) a
(B) b
(C) c
(D) a dan b
(E) a dan c
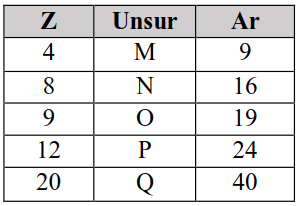
Manakah unsur-unsur yang jika berpasangan membentuk senyawa bersifat paling basa...
(A) M dan N
(B) M dan O
(C) N dan O
(D) N dan P
(E) P dan Q
Reaksi yang tidak dapat menghasilkan asam asetat adalah
(A) oksidasi asetaldehida
(B) oksidasi etanol
(C) hidrolisis asetilamina
(D) hidrolisis etilasetat
(E) oksidasi isopropanol
Unsur yang dapat membentuk ion bermuatan −2 adalah...
(A) 12.
(B) 13.
(C) 14.
(D) 16.
(E) 20.
Jika unsur X dan Y bersenyawa, bentuk molekul senyawa yang terjadi adalah...
(A) jungkat−jungkit.
(B) bentuk V.
(C) piramida segitiga.
(D) bujur sangkar.
(E) segitiga planar.
$Sn + Sr^{2+} \rightarrow$ tidak bereaksi
$Sn + Pd^{2+} \rightarrow Sn^{2+} + Pd$
$Sn + Hg^{2+} \rightarrow Sn^{2+} Hg$
$Sr + Rb^{+} \rightarrow$ Tidak bereaksi
$Hg + Pd^{2+} \rightarrow Hg^{2+} + Pd$
Urutan logam-logam tersebut berdasarkan sifat oksidator yang semakin meningkat adalah ...
(A) Sn < Pd < Hg < Sr < Rb.
(B) Pd < Hg < Sn < Sr < Rb.
(C) Pd < Hg < Sr < Rb < Sn.
(D) Hg < Sn < Sr < Rb < Pd.
(E) Rb < Sr < Sn < Hg < Pd.
Yang paling menentukan reaksi...
(A) proses dari A ke B adalah Endoterm.
(B) proses dari A ke B adalah Eksoterm.
(C) proses dari B ke C adalah Eksoterm.
(D) proses dari B ke C adalah Endoterm.
(E) proses dari A ke C adalah Eksoterm.
Besarnya perubahan entalpi, ΔH seperti pada gambar adalah...
(A) −110,5.
(B) −283,0.
(C) −393,5.
(D) +110,5.
(E) +283,0.
Jika pada menit ke-3 ditambahkan N2, maka...
(A) kesetimbangan bergeser ke arah reaktan.
(B) N2 bertambah.
(C) NH3 bertambah.
(D) H2 bertambah.
(E) tidak terjadi pergeseran kesetimbangan.
Diberikan struktur molekul untuk guanin dan sitosin sebagai berikut.
Jumlah ikatan hidrogen yang dapat terbentuk antara molekul guanin dan sitosin adalah
(A) 1.
(B) 2.
(C) 3.
(D) 4.
(E) 5.
Perhatikan struktur molekul berikut!
Bentuk molekul di sekitar atom N yang mengikat dua atom H adalah...
(A) linier.
(B) bentuk V.
(C) bentuk T.
(D) segitiga planar.
(E) piramida segitiga.
Unsur yang dapat mempunyai bilangan oksidasi +7 dalam senyawanya adalah...
(A) P.
(B) Q.
(C) R.
(D) S.
(E) T.
Perhatikan gambar berikut !
Proses yang menjadi tahap penentu laju reaksi adalah...
(A) proses endoterm dari A ke B.
(B) proses eksoterm dari A ke B.
(C) proses eksoterm dari B ke C.
(D) proses endoterm dari B ke C.
(E) proses eksoterm dari A ke C.
Anda telah membaca artikel Soal UTBK 2019 Kimia dan Pembahasan. Semoga postingan Soal UTBK 2019 Kimia dan Pembahasan ini bisa bermanfaat. Dan jangan lupa bagikan postingan ini di media sosial teman-teman, agar ilmu yang diperoleh dari postingan ini menjadi berkah dan bisa bermanfaat untuk teman-teman yang lain. Terima kasih.























Posting Komentar untuk "Soal UTBK 2019 Kimia + Pembahasan"
Posting Komentar
Silahkan tuliskan komentar Anda sesuai dengan topik postingan halaman ini. Centang "Beri tahu saya" untuk mendapatkan pemberitahuan balasan komentar anda.